Эукариотические клетки способны изменять свою форму, перемещаться, передвигать органеллы по цитоплазме и разделять хромосомы во время митоза. Эта способность обеспечивается трехмерной сетью белковых нитей (филаментов), составляющих главную архитектуру клетки – цитоскелет (иногда обозначаемый как цитоматрикс). Белковые волокна пронизывают цитоплазму эукариотических клеток и во множестве точек связаны с белками плазматической мембраны и органелл. Все эти волокна представляют собой структуры, состоящие из субъединиц – особых глобулярных белков. (Белки цитоскелета, как и другие белки клетки, закодированы в генах и синтезируются на рибосомах.)
Субъединицы цитоскелета соединяются между собой слабыми связями (водородными, ионными и др.) и это свойство позволяет клетке формировать легко изменяющиеся динамичные пространственные структуры цитоскелета. Отмечено, что при различных воздействиях клетка в первую очередь перестраивает цитоскелет, демонтируя основные компоненты своей архитектуры, а затем формирует их заново, в соответствии с характером полученного сигнала; при этом детальное строение цитоскелета постоянно меняется при сохранении общего плана его организации. Такую форму работы цитоскелетной системы называют принципом динамической нестабильности.
В зависимости от диаметра филаменты разделяются на три группы: микрофиламенты (5–7 нм), промежуточные волокна (около 10 нм) и микротрубочки (около 25 нм). Каждый тип цитоскелетных структур образует в клетке собственную систему со своими основными и минорными белками. Эти системы не являются абсолютно независимыми, а взаимодействуют друг с другом и с другими компонентами клетки – плазматической мембраной, ядром и другими органоидами клетки. Согласно существующим представлениям, цитоскелет не только способствует поддержанию формы клетки и осуществляет все типы клеточных движений, но и объединяет разные части клетки и обеспечивает передачу сигналов внутри клетки за счет образования пространственных белковых комплексов между рецепторами и ферментами.
Микрофиламенты встречаются практически во всех типах клеток и состоят из белка актина – наиболее распространенного в эукариотических клетках. (Актин составляет около 5% общего белка клетки; в скелетных мышцах – приблизительно 20% клеточной массы.) Актин может существовать в виде мономера (G-актин – «глобулярный актин», состоящий из 375 аминокислотных остатков) или волокна (F-актин – «фибриллярный актин»). Каждый F-актиновый филамент представляет спиралевидную структуру длиной несколько микрометров. Волокна F-актина имеет два разноименно заряженных конца, которые полимеризуются с различной скоростью. Быстро растущий конец называется плюс-концом, а медленно растущий – минус-концом. Плюс-конец актинового филамента растет в 10 раз быстрее, чем минус-конец.
Микрофиламенты участвуют в динамических процессах, таких, как мышечное сокращение, движение немышечных клеток, фагоцитоз, образование выростов цитоплазмы у подвижных клеток и акросом в процессе слияния сперматозоида с яйцеклеткой. Все эти процессы осуществляются с помощью актин-связывающих белков.
В цитоплазме клеток имеются более 50 различных типов актин-связывающих белков, которые специфически взаимодействуют с G-актином и F-актином. Эти белки выполняют различные функции: регулируют объём G- актинового пула (профилин), стабилизируют концы нитей F-актина (фрагин), сшивают филаменты с другими компонентами цитоскелета. Некоторые актин-связывающие белки, например, гельформирующие (от слова – желе) – скрепляют волокна актина крест-накрест и, тем самым, переводят состояние участка цитоплазмы из состояния золь (от лат. solutio – раствор) в гель. Ещё один актин-связывающий белок – спектрин, называемый также фодрином, соединяет волокна актина в пучки и прикрепляет их к цитоплазматической мембране и к сетке, построенной из промежуточных волокон. Белок валлин сцепляет актиновые филаменты в параллельно упорядоченные жесткие структуры и оказывает влияние на скорость полимеризации G-актина.
Почти все типы движений в клетке происходят с участием актин-связывающего белка миозина. У всех молекул миозина имеется головка, шейка и хвост. Головка миозина способна присоединяться к мономеру актина и, при наличии АТФ, двигаться от плюс- к минус-концу микрофиламента. В скелетных мышцах молекулы актина и миозина расположены на фиксированных расстояниях друг от друга, а перемещение головок миозина по актиновым нитям приводит к сокращению мышц. В немышечных клетках при взаимодейстии с белком миозином актиновые филаменты могут формировать сократительные пучки, благодаря которым образуются инвагинации (впячивания) клеточной поверхности. Такие инвагинации образуются, например, при делении клеток. В общем, характер движений в клетке зависит от строения белка миозина, структура которого имеет более 80 вариантов. Комбинируя актиновые микрофиламенты с различными вариантами миозина и другими актин-связывающими белками, клетка формирует структуры, различающиеся по архитектуре, подвижности и времени существования.
У большинства клеток микрофиламенты образуют под плазматической мембраной трехмерную структуру, так называемую актиновую кору (актиновый кортекс). Особенность этой структуры – быстрое обновление микрофиламентов; например, в кортексе лейкоцита филаменты существуют не более 5 секунд. Основной тип перестроек кортекса у подвижных клеток связан с образованием
псевдоподий – выростов цитоплазмы. Псевдоподии могут иметь форму плоской пластинки (ламеллоподия), узкого цилиндра (филоподия) или шаровидного пузыря. Форма псевдоподий зависит от типа актин-связывающих белков, взаимодействующих с микрофиламентами и плазматической мембраной.
Актиновые микрофиламенты участвуют также в создании сложных пространственных и относительно стабильных цитоскелетных структур. Например, основу микроворсинок эпителиальных клеток кишечника и почек составляют длинные пучки актиновых филаментов. На верхней поверхности волосковых клеток улитки внутреннего уха, отвечающих за восприятие звуков, находятся специализированные отростки (волоски) – стереоцилии. Стереоцилии располагаются правильными рядами подобно трубам клавишно-музыкального инструмента – оргáна. Внутренняя полость волоска-стереоцилии заполнена актиновыми филаментами и молекулами других белков. Мутации некоторых генов, кодирующих эти белки, приводит к дегенерации волосковых клеток и проявляется в виде одной из форм наследственной глухоты (синдром Ашера).
Микрофиламенты принимают активное участие в движении клетки. При этом актиновые филаменты постоянно полимеризуется на конце двигательного края клетки и деполимеризуется с внутренней стороны. Процессы полимеризации и деполимеризации F-актина могут быть нарушены ядами (токсинами) грибов. Например, фаллоидин (яд бледной поганки) связывается с минус-концом актина и ингибирует деполимеризацию, в то время как цитохалазин (токсин из плесневых грибов, обладающий свойством цитостатика) присоединяется к плюс-концу, блокируя полимеризацию актина и движение клетки. Длительное воздействие веществ, нарушающих полимеризацию или деполимеризацию актиновых филаментов, приводит к смерти этих клеток.
Полимеризация актина – это точно регулируемый процесс, контролируемый с помощью поверхностных рецепторов клетки, ферментов (протеинкиназ) и ионов кальция. Нарушение этого процесса сопровождается клиническими проявлениями. Например, в трансформированных клетках отмечается уменьшение экспрессии белков, регулирующих сборку актина. Значительные аномалии актиновых филаментов наблюдаются в клетках некоторых злокачественных опухолей. В клетках саркомы (опухоли соединительной ткани) обнаружено наличие тонких и коротких филаментов актина. Эти клетки, в отличие от нормальных клеток, очень подвижны и обладают большой способностью к метастазированию.
Промежуточные филаменты состоят из белков специфических для определенных клеточных типов (напр. кератины в эпителиальных клетках, виментин в клетках соединительной ткани, десмин в клетках мышечных тканей и др). Промежуточные филаменты придают прочность клетке, так как они представляют собой крепкие, волокнистые, устойчивые к растяжению полипептиды и распределяются по всей цитоплазме клетки, образуя прочную сеть. Кроме того, промежуточные волокна присутствуют в ядре, образуя сеть филаментов (ламину) на внутренней поверхности ядерной мембраны, тесно связанную с ядерными порами.
Структурными элементами промежуточных волокон являются белки, принадлежащие к пяти родственным семействам и проявляющие высокую степень клеточной специфичности. Типичными представителями этих белков являются цитокератины, десмин, виментин, кислый фибриллярный глиапротеин и нейрофиламент. Все эти белки имеют в центральной части базовую стержневую структуру, которая носит название α-спирали. Две пептидные цепи (димер) образуют суперспираль. Такие димеры соединяются антипараллельно, образуя тетрамер. Агрегация тетрамеров по принципу «голова к голове» даёт протофиламент. Восемь протофиламентов сплетаются вместе и образуют промежуточное волокно диаметром 10 нм. Эластичность промежуточных филаментов обеспечивается тем, что димеры каждого тетрамера расположены в шахматном порядке относительно друг друга.
Волосы и ногти человека, шерсть, перья, иглы, когти, и копыта животных состоят главным образом из кератина (цитокератина). В одном волокне шерсти переплетены миллионы фибрилл. Отдельные цепи кератина скреплены многочисленными дисульфидными связями, что придает им дополнительную твердость. Выделено более 30 различных кератинов, комбинирующихся по два типа в эпителиальных клетках человека. Кроме того описано восемь изоформ тяжелых кератинов, специфичных для волос и ногтей. В нервных клетках существуют нейрофиламенты, придающие необходимую механическую опору длинным аксонам. Филаменты десмина расположены в Z-дисках саркомеров скелетных мышц. В различных типах клеток промежуточные филаменты играют важную роль в формировании клеточных контактов, называемых десмосомами, которые соединяют соседние клетки. Полудесмосомы прикрепляют эпителиальные клетки к базальной мембране, на которой они расположены.
Микротрубочки
Присутствующие во всех эукариотических клетках микротрубочки представляют собой длинные нитевидные структуры, протянутые по всей цитоплазме и формирующие сеть, которая поддерживает структурную организацию и локализацию некоторых органелл.
Микротрубочки образуются при полимеризации белка тубулина (лат. tubula – трубочка), который является гетеродимером, образованным субъединицами α- и β- тубулина. В процессе полимеризации α -тубулин одного димера контактирует сβ -тубулином следующего димера с образованием протофиламентов. Тринадцать тубулиновых продольных рядов протофиламентов (нитей), идущих по спирали, образуют микротрубочку диаметром 24 нм и длиной несколько микрометров.
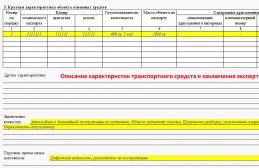
Рис. Схема строения микротрубочки, показывающая каким образом тубулиновые полипептиды, связываясь друг с другом, образуют цилиндрическую стенку. А. Поперечный срез Б – Короткий отрезок микротрубочки.
Микротрубочки способны образовывать синглет
, дублет
и триплет
.
A
микротрубочка дублета или триплета состоит из 13 протофиламентов.
Трубочки B
и C
состоят из меньшего числа протофиламентов, обычно 10.

Полимеризация микротрубочек происходит в направлении от головы к хвосту таким образом, что микротрубочка имеет определенную полярность: её концы обозначаются соответственно как плюс- и минус-концы. Микротрубочки в клетке нестабильны. Они могут быстро собираться и разбираться. В клетке минус-концы связаны с центром организации микротрубочек (ЦОМТ) – структурой, расположенной около ядра, которая содержит в животных клетках пару маленьких телец – центриолей, образованных из слившихся микротрубочек. Как правило, микротрубочки ассоциированы с другими белками (миозин, динеин, кинезин), которые связывают микротрубочки с другими элементами цитоскелета и органеллами. Кинезин обеспечивает транспорт органелл и везикул (пузырьков) из одной части клетки в другую от плюс-конца микротрубочки к минус-концу, а динеин от минус-конца к плюс-концу.
Известны химические соединения, способные блокировать сборку микротрубочек (колхицин, винбластин) и стимулирующие образование стабильных микротрубочек (таксол). Следует отметить, что в развивающемся организме могут сложиться условия (недостаток кислорода, пониженная или повышенная температура и т.д.), когда нарушается сборка микротрубочек в клетках, это может служить причиной отклонения от нормального развития.
Микротрубочки, как и актиновые филаменты, принимают участие в поддержании формы клетки. Наряду со статической функцией, микротрубочки участвуют во многих процессах, протекающих во всех эукариотических клетках: мейозе, митозе, клеточном движении и секреции. Они служат направляющими «рельсами» для транспорта органелл. Вместе с ассоциированными белками микротрубочки способны осуществлять механическую работу, например, транспорт митохондрий, перемещение синаптических пузырьков, движение ресничек (волосоподобных выростов клеток в эпителии легких, кишечника и яйцеводов) и биение жгутика сперматозоида. Пузырьки, образуемые аппаратом Гольджи, направляются в различные места клетки по микротрубочкам строго по назначению. Кроме того микротрубочки в форме митотического веретена – важнейшая часть аппарата, обеспечивающего правильное распределение хромосом между дочерними клетками при делении эукариотических клеток.
Функции микротрубочек: 1) обеспечение расхождения хромосом при делении клеток, 2) поддержание формы клетки, 3) участие в транспорте макромолекул и органелл, 4) обеспечение подвижности жгутиков, ресничек.
Функции цитоскелета
Цитоскелет выполняет три главные функции.
1. Служит клетке механическим каркасом, который придаёт клетке типичную форму и обеспечивает связь между мембранной и органеллами. Каркас представляет собой динамичную структуру, которая постоянно обновляется по мере изменения внешних условий и состояния клетки.
2. Действует как «мотор» для клеточного движения. Двигательные (сократительные) белки содержатся не только в мышечных клетках, но и в других тканях. Компоненты цитоскелета определяют направление и координируют движение, деление, изменение формы клеток в процессе роста, перемещение органелл, движение цитоплазмы.
3. Служит в качестве «рельсов» для транспорта органелл и других крупных комплексов внутри клетки.
Микрофиламенты и промежуточные волокна.
Микрофиламенты построенные из F-актина пронизывают микроворсинки, образуя узлы. Эти микроволокна удерживаются вместе с помощью актинсвязывающих белков, наиболее важными из которых являются фимбрин и виллин. Кальмодулин и миозиноподобная АТФ – аза соединяют крайние микроволокна с плазматической мембраной. .
Клетка может менять набор синтезируемых белков цитоскелета в зависимости от условий, но процесс этот медленный. Конструкция цитоскелета способна быстро меняться даже без синтеза новых молекул, за счет полимеризации и деполимеризации нитей. В клетке все время идет обмен между нитями и раствором белков-мономеров в цитоплазме. Во многих клетках примерно половина молекул актина и тубулина находится в виде мономеров в цитоплазме и половина входит в состав нитей микрофиламентов. Клетка регулирует стабильность нитей цитоскелета, присоединяя к ним специальные белки, изменяющие скорость полимеризации. Общий принцип функционирования цитоскелета – динамическая нестабильность. Например, форму эритроцита в виде двояковогнутого диска поддерживает примембранный цитоскелет из волокон, образованных белком спектрином. Спектрин связан с белком анкерином (anchor – якорь), который соединяется с белком цитоплазматической мембраны, ответственным за транспорт анионов (Cl - , HCO - 3). Дефекты белков спектрина и анкирина вызывают необычную форму эритроцитов. Такие эритроциты очень быстро разрушаются в селезенке. Болезни, вызываемые такими нарушениями, называют наследственным сфероцитозом или наследственным эллиптоцитозом.

Рис. Цитоскелет эукариот. Актиновые микрофиламенты окрашены в красный, микротрубочки - в зеленый, ядра клеток - в голубой цвет.

Цитоскелет образуется тремя компонентами: микротрубочками, микрофиламентами, и промежуточными филаментами.
Микротрубочки пронизывают всю цитоплазму клетки. Каждая из них представляет собой полый цилиндр диаметром 20 – 30 нм. Стенка микротрубочек образована 13-ю нитями (протофиламентами), скрученными по спирали одна над другой. Каждая нить, в свою очередь, слагается из димеров белка тубулина. Синтез тубулинов происходит на мембранах гранулярной ЭПС, а сборка в спираль – в клеточном центре.
Соответственно, многие микротрубочки имеют радиальное направление по отношению к центриолям. Отсюда они распространяются по всей цитоплазме.
Большинство микротрубочек имеет закрепленный («-») и свободный («+») концы.Свободный конец обеспечивает удлинение и укорочение трубочек.В образовании микротрубочек путем самосборки участвуют мелкие сферические тельца – сателлиты (центры организации микротрубочек), содержащиеся в клеточном центре и в базальных тельцах ресничек, а также центромеры хромосом. Если полностью разрушить микротрубочки цитоплазмы, то они отрастают от клеточного центра со скоростью 1 мкм/мин. Разрушение микротрубочек приводит к изменению формы клетки (животная клетка обретает обычно сферическую форму). При этом нарушаются структура клетки и распределение органелл.
В клетке микротрубочки могут располагаться:
Ø в виде отдельных элементов;
Ø в пучках, в которых они связаны друг с другом поперечными мостиками (отростки нейронов);
Ø в составе пар или дублетов (осевая нить ресничек и жгутиков);
Ø в составе триплетов (центриоли и базальные тельца).
В двух последних вариантах микротрубочки частично сливаются друг с другом.
Функции микротрубочек:
а) поддержание формы и полярности клетки;
б) обеспечение упорядоченности расположения компонентов клетки;
в) участие в образовании других, более сложных органелл (центриоли, реснички и т.д.);
г) участие во внутриклеточном транспорте;
д) обеспечение движения хромосом при митотическом делении клетки;
е) обеспечение движения ресничек.
Микрофиламенты. Микрофиламентами названы тонкие белковые нити диаметром 5 – 7 нм, встречающиеся практически во всех типах клеток. Они могут располагаться в цитоплазме пучками, сетевидными слоями или поодиночке.
Основным белком микрофиламентов является актин,на долю которого приходится до 5% от общего количества белков. Кроме него в состав микрофиламентов могут входить миозин, тропомиозин, а также несколько десятков актинсвязывающих белков. Молекула актина имеет обычно вид двух спирально скрученных нитей. Непосредственно под плазмолеммой располагается кортикальная сеть,в которой микрофиламенты переплетены между собой и соединены друг с другом с помощью особых белков, например филамина. Кортикальная сеть обусловливает плавность изменения формы клеток, постепенно перестраиваясь с участием актин-расщепляющих ферментов.Тем самым она препятствует резкой и внезапной деформации клетки при механических воздействиях. Отдельные микрофиламенты кортикальной сети прикрепляются к интегральным и трансмембранным белкам плазмолеммы, а также к так называемым адгезионным соединениям (фокальным контактам), которые связывают клетку с компонентами межклеточного вещества или с другими клетками. Микрофиламенты более устойчивы к физическим и химическим воздействиям, чем микротрубочки.
Основные функции микрофиламентов:
1) обеспечение определенной жесткости и упругости клетки за счет кортикальной сети микрофиламентов;
2) изменение консистенции цитозоля, в том числе при переходе золя в гель;
3) участие в эндоцитозе и экзоцитозе;
4) обеспечение подвижности немышечных клеток (например, нейтрофилов и макрофагов), в основе которой лежит изменение формы клеточной поверхности вследствие регулируемой полимеризации актина;
5) участие в сокращении мышечных клеток и волокон;
6) стабилизация локальных выпячиваний плазматической мембраны, обеспечиваемой пучками поперечно сшитых актиновых филаментов (микроворсинки, стереоцилии);
7) участие в формировании межклеточных соединений (опоясывающие десмосомы и др.).
Промежуточные филаменты представляют собой сплетенные белковыми нитями канаты толщиной около 10 нм. Такой показатель обусловил отведение им промежуточного места между микротрубочками и микрофиламентами. Промежуточные филаменты образуют трехмерные сети в клетках различных тканей животного организма. Они окружают ядро и могут находиться в различных участках цитоплазмы, образуют межклеточные соединения (десмосомы и полудесмосомы), располагаются внутри отростков нервных клеток.
Основные функции промежуточных филаментов:
1) структурная;
2) опорная;
3) функция распределения органелл в определенных участках клетки.
ЦИТОСКЕЛЕТ
Цитоскелет представляет собой сложную динамичную систему микротрубочек, микрофиламентов, промежуточных филаментов и микротрабекул. Указанные компоненты цитоскелета являются немем-" бранными органеллами; каждый из них образует в клетке трехмерную сеть с характерным распределением, которая взаимодействует с сетями из других компонентов. Они входят также в состав ряда других более сложно организованных органелл (ресничек, жгутиков, микроворсинок, клеточного центра) и клеточных соединений (десмосом, полудесмосом, опоясывающих десмосом).
Основные функции цитоскелета:
1 поддержание и изменение формы клетки;
2 распределение и перемещение компонентов клетки;
3 транспорт веществ в клетку и из нее;
4 обеспечение подвижности клетки;
5участие в межклеточных, соединениях.
Микротрубочки
Микротрубочки, - наиболее крупные компоненты цитоскелета. Они представляют с^бой полые цилиндрические образования, имеющие форму трубочек, длиной до нескольких микрометров (в жгутиках более 50 нм) диаметром около 24-25 нм, с толщиной стенки 5 нм и диаметром просвета 14-15 нм (рис. 3-14).
Стенка микротрубочки состоит из спиралевидно уложенных нитей - протофиламентов толщиной 5 нм (которым на поперечном разрезе соответствуют 13 субъединиц), образованных димерами из белковых молекул а~ и /3-тубулина.
Функции микротрубочек:
(1) поддержание формы и полярности клетки, распределения ее компонентов,
(2) обеспечение внутриклеточного транспорта,
(3) обеспечение движения ресничек, хромосом в митозе (формируют ахроматиновое веретено, необходимое для клеточного деления),
(4) образование основы других органелл (центриолей, ресничек).
Расположение микротрубочек. Микротрубочки располагаются в цитоплазме в составе нескольких систем;
а) в виде отдельных элементов, разбросанных по всей цитоплазме и формирующих сети;
б) в пучках, где они связаны тонкими поперечными мостиками (в отростках нейронов, в составе митогяческого веретена, манжетки сперматиды, периферического "кольца" тромбоцитов);
в) частично сливаясь друг с другом с формированием пар, или дублетов (в аксонеме ресничек и жгутиков), и триплетов (в базальном тельце и центриоли).
Образование и разрушение микротрубочек. Микротрубочки представляют собой лабильную систему, в которой имеется равновесие между их постоянной сборкой и диссоциацией. У большинства микротрубочек один конец (обозначаемый как "-") закреплен, а другой ("+") свободен и участвует в их удлинении или деполимеризации. Структурами, обеспечивающими образование микротрубочек, служат особые мел- I кие сферические тельца - сателлиты (от англ, satellite - спутник), отче- { го последние называют центрами организации микротрубочек (ЦОМТ). . Сателлиты содержатся в базалъных тельцах ресничек и клеточном цен- I тре (см. рис. 3-15 и 3-16). После полного разрушения микротрубочек ] в цитоплазме они отрастают от клеточного центра со скоростью около 1 мкм/мин., а их сеть вновь восстанавливается менее, чем за полтора часа. К ЦОМТ относят также и центромеры хромосом.
Связь микротрубочек с другими структурами клетки и между собой осуществляется посредством ряда белков, выполняющих различные функции. (1) Микротрубочки с помощью вспомогательных белков прикреплены к другим клеточным компонентам. (2) По своей длине микротрубочки образуют многочисленные боковые выросты (которые состоят из белков, ассоциированных с микротрубочками) длиной до нескольких десятков нанометров. Благодаря тому, что такие белки последовательно и обратимо связываются с органеллами, транспортными пузырьками, секреторными гранулами и другими образованиями, микротрубочки (ко- ] торые сами не обладают сократимостью) обеспечивают перемещение указанных структур по цитоплазме. (3) Некоторые белки, ассоциированные с микротрубочками, стабилизируют их структуру, а связываясь с их свободными краями, препятствуют деполимеризации.
Угнетение самосборки микротрубочек посредством ряда веществ, являющихся ингибиторами митоза (колхицин, винбластин, винкрис-тин), вызывает избирательную гибель быстроделящихся клеток. Поэтому некоторые из таких веществ успешно используются для химиотера-
пии опухолей. Блокаторы микротрубочек нарушают также транспортные процессы в цитоплазме, в частности, секрецию, аксонный транспорт в нейронах. Разрушение микрогрубочек приводит к изменениям формы клетки и дезорганизации ее структуры и распределения органелл.
Клеточный центр (цитоцентр)
Клеточный центр образован двумя полыми цилиндрическими структурами длиной 0.3-0.5 <мкм и диаметром 0.15-0.2 мкм - центриоля-ми, которые располагются вблизи друг друга во взаимно перпендикулярных плоскостях (рис. 3-15). Каждая центриоль состоит из 9 триплетов частично слившихся микротрубочек (А, В и С), связанных поперечными белковыми мостиками ("ручками"). В центральной части центриоли микротрубочки отсутствуют (по некоторым данным, здесь имеется особая центральная нить), что описывается общей формулой (9*3) + 0. Каждый триплет центриоли связан со сферическими тельцами диаметром 75 нм - сателлитами; расходящиеся от них микротрубочки образуют центросферу.
В неделящейся клетке выявляется одна пара центриолей (диплосо-ма), которая обычно располагается вблизи ядра. Перед делением в S-ne-риоде интерфазы происходит дупликация центриолей пары, причем под прямым углом к каждой зрелой (материнской) центриоли формируется новая (дочерняя), незрелая процентриоль, в которой вначале имеются лишь 9 единичных микротрубочек, позднее превращающихся в триплеты. Пары центриолей далее расходятся к полюсам клетки, а во время митоза они служат центрами образования микротрубочек ахроматина-вого веретена деления.
Реснички и жгутики
Реснички и жгутики - органеллы специального значения, участвующие в процессах движения, - представляют собой выросты цитоплазмы, основу которых составляет каркас из микротрубочек, называемый осевой нитью, или аксонемой (от греч. axis - ось и пета - нить). Длина ресничек равна 2-10 мкм, а их количество на поверхности одной реснитчатой клетки может достигать нескольких сотен. В единственном типе клеток человека, имеющих жгутик - спермиях - содержится только по одному жгутику длиной 50-70 мкм.
Аксонема образована 9 периферическими парами микротрубочек и одной центрально расположенной парой; такое строение описывается формулой (9 х 2) + 2 (рис. 3-16). Внутри каждой периферической пары за счет частичного слияния микротрубочек одна из них (А) полная, а вторая (В) - неполная (2-3 димера общие с микротрубочкой А).
Центральная пара микротрубочек окружена центральной оболочкой, от которой к периферическим дублетам расходятся радиальные спицы. Периферические дублеты связаны друг с другом мостиками нек-сина, а от микротрубочки А к микротрубочке В соседнего дублета отходят "ручки" из белка динеина (см. рис. 3-16), который обладает активностью АТФазы.
Биение реснички и жгутика обусловлено скольжением соседних дублетов в аксонеме, которое опосредуется движением динеиновых ручек. Мутации, вызывающие изменения белков, входящих в состав ресничек и жгутиков, приводят к различным нарушениям функции соответствующих клеток. При синдроме Картагенера (синдроме неподвижных, ресничек), обычно обусловленном отсутствием динеиновых ручек, больные страдают хроническими заболеваниями дыхательной системы (связанными с нарушением функции очищения поверхности респираторного эпителия) и бесплодием (вследствие неподвижности спермиев).
Базальное тельце, по своему строению сходное с центриолью, лежит в основании каждой реснички или жгутика. На уровне апикального конца тельца микротрубочка С триплета заканчивается, а микротрубочки А и В продолжаются в соответствующие микротрубочки аксоне-мы реснички или жгутика. При развитии ресничек или жгутика базаль-ное тельце играет роль матрицы, на которой поисходит сборка компонентов аксонемы.
Микрофиламенты
Микрофиламенты - тонкие белковые нити диаметром 5-7 ни, лежащие в цитоплазме поодиночке, в виде сетей или пучками. В скелетной мышце тонкие Микрофиламенты образуют упорядоченные пучки, взаимодействуя с более толстыми миозиновыми филаментами.
Кортикальная (терминальная) сеть - зона сгущения микрофила-ментов под плазмолеммой, характерная для большинства клеток. В этой сети Микрофиламенты переплетены между собой и "сшиты" друг с другом с помощью особых белков, самым распространенным из которых является филамин. Кортикальная сеть препятствует резкой и внезапной деформации клетки при механических воздействиях и обеспечивает плавные изменения ее формы путем перестройки, которая облегчается актин-растворяющими (преобразующими) ферментами.
Прикрепление микрофиламентов к плазмолемме осуществляется благодаря их связи с ее интегральными ("якорными") белками (интег-ринами) - непосредственно или через ряд промежуточных белков - талин, винкулин и сс-актинин (см. рис. 10-9). Помимо этого, актиновые микрофиламенты прикрепляются к трансмембранным белкам в особых участках плазмолеммы, называемых адгезионными соединениями, или фокальными контактами, которые связывают клетки друг с другом или клетки с компонентами межклеточного вещества.
Актин - основной белок микрофиламентов - встречается в мономерной форме (G -, или глобулярный актин), которая способна в присутствии цАМФ и Са 2+ полимеризоваться в длинные цепи (F -, или фибриллярный актин). Обычно молекула актина имеет вид двух спирально скрученных нитей (см. рис. 10-9 и 13-5).
В микрофиламентах актин взаимодействует с рядом актин-связы-вающих белков (до нескольких десятков видов), выполняющих различные функции. Некоторые из них регулируют степень полимеризации актина, другие (например, филамин в кортикальной сети или фимбрин и виллин в микроворсинке) способствуют связыванию отдельных микрофиламентов в системы. В немышечных клетках на актин приходится примерно 5-10% содержания белка, лишь около половины его организовано в филаменты. Микрофиламенты более устойчивы к физическим и химическим воздействиям, чем микротрубочки.
Функции микрофиламентов:
(1) обеспечение сократимости мышечных клеток (при взаимодействии с миозином);
(2) обеспечение функций, связанных с кортикальным слоем цитоплазмы и плазмолеммой (экзо- и эндоцитоз, образование псевдоподий и миграция клетки);
(3) перемещение внутри цитоплазмы ореанелл, транспортных пузырьков и других структур благодаря взаимодействию с некоторыми белками (минимиозином), связанными с поверхностью этих структур;
(4) обеспечение определенной жесткости клетки за счет наличия кортикальной сети, которая препятствует действию деформаций, но сама, перестраиваясь, способствует изменениям клеточной формы;
(5) формирование сократимой перетяжки при цитотомии, завершающей клеточное деление;
(6) образование основы ("каркаса") некоторых органелл (микро-ворсинок, стереоцилий).
(7) участие в организации структуры межклеточных соединений (опоясывающих десмосом).
Микроворсинки - пальцевидные выросты цитоплазмы клетки диаметром 0.1 мкм и длиной 1 мкм, основу которых образуют актиновые микрофиламенты. Микроворсинки обеспечивают многократное увеличение площади поверхности клетки, на которой происходит расщепление и всасывание веществ. На.апикальной поверхности некоторых клеток, активно участвующих в указанных процессах (в эпителии тонкой кишки и почечных канальцев) имеется до нескольких тысяч микроворсинок, образующих в совокупности щеточную каемку.
Каркас каждой микроворсинки образован пучком, содержащим около 40 микрофиламентов, лежащих вдоль ее длинной оси (рис. 3-17). В апикальной части микроворсинки этот пучок закреплен в аморфном веществе. Его жесткость обусловлена поперечными сшивками из белков фимбрина и виллина, изнутри пучок прикреплен к плазмолемме Микроворсинки особыми белковыми мостиками (молекулами минимио- З ина). У основания микроворсинки микрофиламенты пучка вплетается в терминальную сеть, среди элементов которой имеются миозиновые филаменты. Взаимодействие актиновых и миозиновых филаментов терминальной сети, вероятно, обусловливает тонус и конфигурацию микроворсинки.
Стереоцилии - видоизмененные длинные (в некоторых клетках -ветвящиеся) микроворсинки - выявляются значительно реже, чем микроворсинки и, подобно последним, содержат пучок микрофиламентов.
Цитоскелет - это совокупность нитевидных белковых структур находящихся в цитоплазме живой клетки и образующих клеточный скелет или каркас. В 2001 году было установлено, что цитоскелет есть и в эукариотичских и прокариотических клетках. До 2001 года считалось то, что прокариотические клетки не имеют цитоскелета. Выделяют несколько основных систем цитослекелета клетки, которые делятся по основным белкам, входящим в состав (кератины, тубулин-динеиновая система или актин-миозиновая система) или по основным структурным элементам, заметным при электронно-микроскопических исследованиях (микрофиламенты, микротрубочки или промежуточные филаменты).
Функции цитоскелета
Цитоскелет выполняет следующие функции:
1. Из названия цитоскелет можно понять его главную функцию. Он является скелетом или каркасом клетки;
2. Он придаёт клетке определённую форму и обеспечивает внутри клетки перемещение и взаимодействие органелл;
3. Цитоскелет может изменяться при изменении внешних условий и состояния клетки;
4. За счёт измененеия структуры обеспечивает движение цитоплазмы, изменение формы клеток в процессе роста.
Из определения цитоскелета можно понять, что цитоскелет клетки состоит из белков трёх разных видов. В состав цитосклета входят микрофиламенты, промежуточные филаменты и микротрубочки.
1. Микрофиламентами называются нити, состоящие из молекул глобулярного белка актина, миозина, тропомиозина, актинина. Имеют размер 7-8 нанометров. Состоят из двух перекрученных цепочек белка;
2. Промежуточными филаментами называются нитевидные структуры из особых белков четырёх типов. Имеют размер 9-11 нанометров;
3. Микротрубочками цитоскелета называют белковые структуры представляющие собой полые цилиндры образованные димерами тубулина. Диаметр цилиндр равен 25 нанометрам. Микротрубочки как и микрофиламенты являются полярными.
Цитоскелет
Цитоскелет эукариот. Актиновые микрофиламенты окрашены в красный, микротрубочки - в зелёный, ядра клеток - в голубой цвет.
Цитоскеле́т - это клеточный каркас или скелет, находящийся в цитоплазме живой клетки . Он присутствует во всех клетках эукариот , причем в клетках прокариот обнаружены гомологи всех белков цитоскелета эукариот. Цитоскелет - динамичная, изменяющаяся структура, в функции которой входит поддержание и адаптация формы клетки ко внешним воздействиям, экзо- и эндоцитоз, обеспечение движения клетки как целого, активный внутриклеточный транспорт и клеточное деление.

Кератиновые промежуточные филаменты в клетке.
Цитоскелет образован белками, выделяют несколько основных систем, называемых либо по основным структурным элементам, заметным при электронно-микроскопических исследованиях (микрофиламенты , промежуточные филаменты , микротрубочки), либо по основным белкам, входящим в их состав (актин -миозиновая система, кератины , тубулин -динеиновая система).
Цитоскелет эукариот
Цитоскелет прокариот
Долгое время считалось, что цитоскелетом обладают только эукариоты . Однако с выходом в 2001 году статьи Jones и соавт. (PMID: 11290328), описывающей роль бактериальных гомологов актина в клетках Bacillus subtilis , начался период активного изучения элементов бактериального цитоскелета. К настоящему времени найдены бактериальные гомологи всех трех типов элементов цитоскелета эукариот - тубулина , актина и промежуточных филаментов . Также было установлено, что как минимум одна группа белков бактериального цитоскелета, MinD/ParA, не имеет эукариотических аналогов.
Бактериальные гомологи актина
К наиболее изученным актиноподобным компонентам цитоскелета относятся MreB, ParM и MamK.
MreB и его гомологи
Белки MreB и его гомологи являются актиноподобными компонентами цитоскелета бактерий, играющими важную роль в поддержании формы клетки, сегрегации хромосом и организации мембранных структур. Некоторые виды бактерий, такие как Escherichia coli , имеют только один белок MreB, тогда как другие могут иметь 2 и более MreB-подобных белков. Примером последних служит бактерия Bacillus subtilis , у которой были обнаружены белки MreB, Mbl (M reB -l ike) и MreBH (MreB h omolog).
В геномах E. coli и B. subtilis ген, отвечающий за синтез MreB, находится в одном опероне с генами белков MreC и MreD. Мутации, подавляющие экспрессию данного оперона, приводят к образованию клеток сферической формы с пониженной жизнеспособностью.
Субъединицы белка MreB образуют филаменты, обвивающие палочковидную бактериальную клетку. Они располагаются на внутренней поверхности цитоплазматической мембраны. Филаменты, образуемые MreB, динамичны, постоянно претерпевают полимеризацию и деполимеризацию. Непосредственно перед делением клетки MreB концентрируется в области, в которой будет формироваться перетяжка. Считается, что функцией MreB также является координация синтеза муреина - полимера клеточной стенки.
Гены, отвечающие за синтез гомологов MreB, были обнаружены только у палочковидных бактерий и не были найдены у кокков.
ParM
Белок ParM присутствует в клетках, содержащих малокопийные плазмиды. Его функция заключается в разведении плазмид по полюсам клетки. При этом субъединицы белка формируют филаменты, вытянутые вдоль большой оси палочковидной клетки.
Филамент по своей структуре представляет собой двойную спираль. Рост филаментов, образуемых ParM, возможен с обоих концов, в отличие от актиновых филаментов, растущих только на ±полюсе.
MamK
MamK - это актиноподобный белок Magnetospirillum magneticum , отвечающий за правильное расположение магнитосом. Магнитосомы представляют собой впячивания цитоплазматической мембраны, окружающие частички железа. Филамент MamK выполняет роль направляющей, вдоль которой, одна за другой, располагаются магнитосомы. В отсутствие белка MamK магнитосомы располагаются беспорядочно по поверхности клетки.
Гомологи тубулина
В настоящее время у прокариот найдены 2 гомолога тубулина: FtsZ и BtubA/B. Как и эукариотический тубулин, эти белки обладают ГТФазной активностью.
FtsZ
Белок FtsZ чрезвычайно важен для клеточного деления бактерий, он найден практически у всех эубактерий и архей. Также гомологи этого белка были обнаружены в пластидах эукариот, что является ещё одним подтверждением их симбиотического происхождения .
FtsZ формирует так называемое Z-кольцо, выполняющее роль каркаса для дополнительных белков клеточного деления. Вместе они представляют собой структуру, ответственную за образование перетяжки (септы) .
BtubA/B
В отличие от широко распространенного FtsZ, эти белки обнаружены только у бактерий рода Prosthecobacter . Они более близки к тубулину по своему строению, чем FtsZ.
Кресцентин, гомолог белков промежуточных филаментов
Белок был найден в клетках Caulobacter crescentus . Его функцией является придание клеткам C. crescentus формы вибриона. В случае отсутствия экспрессии гена кресцентина клетки C. crescentus приобретают форму палочки. Интересно, что клетки двойных мутантов, кресцентин − и MreB − , имеют сферическую форму.
MinD и ParA
Эти белки не имеют гомологов среди эукариот.
MinD отвечает за положение сайта деления у бактерий и пластид. ParA участвует в разделении ДНК по дочерним клеткам.
См. также
Примечания
| Белки цитоскелета | |
|---|---|
| Микрофиламенты | Актинин (1, 2, 3, 4) · Arp2/3 complex · actin depolymerizing factors (Cofilin (1, 2) · Дестрин) · Gelsolin · Profilin (1, 2) · Титин |
| Промежуточные филаменты | первого и второго типа (цитокератин, type I, type II) · третьего типа (десмин , GFAP, Peripherin, виментин) · четвертого типа (Internexin, Nestin, нейрофиламент, Synemin, Syncoilin) · пятого типа (ламин A, B) |
| Микротрубочки | Динеины · Кинезины · Белки, связанные с микротрубочками (Tau protein, Dynamin) · Tubulins · Stathmin · Tektin |
| Катенины | Alpha catenin · Beta catenin · Plakoglobin (gamma catenin) · Delta catenin |
| другие | APC · Dystrophin (Dystroglycan) · plakin (Desmoplakin, Plectin) · Spectrin (SPTA1, SPTAN1, SPTB, SPTBN1, SPTBN2, SPTBN4, SPTBN5) · Talin (TLN1) · Utrophin · Vinculin |
| В этой статье не хватает ссылок на источники информации. |